まず全体像から読みたい方はこちら:→ A0:CAR-T療法とは?まず全体像(目次つき)→ A2:CAR-Tの副作用を怖がらず理解する(何が起きる?何を見守る?)
まず全体像から読みたい方はこちら:
→ A0:CAR-T療法とは?まず全体像(目次つき)
→ A2:CAR-Tの副作用を怖がらず理解する(何が起きる?何を見守る?)
この記事でわかること
- まず結論(エグゼクティブ・サマリー)
- 1) 毒性管理の“座標系”:何を、いつ、どう見て、どう上げるか
- 2) CRS(サイトカイン放出症候群):実務としての見方と介入
- 3) ICANS(神経毒性):家族が気づく“兆候”を医療に落とす
- 4) 退院後運用:感染・血球減少・再来院トリアージ
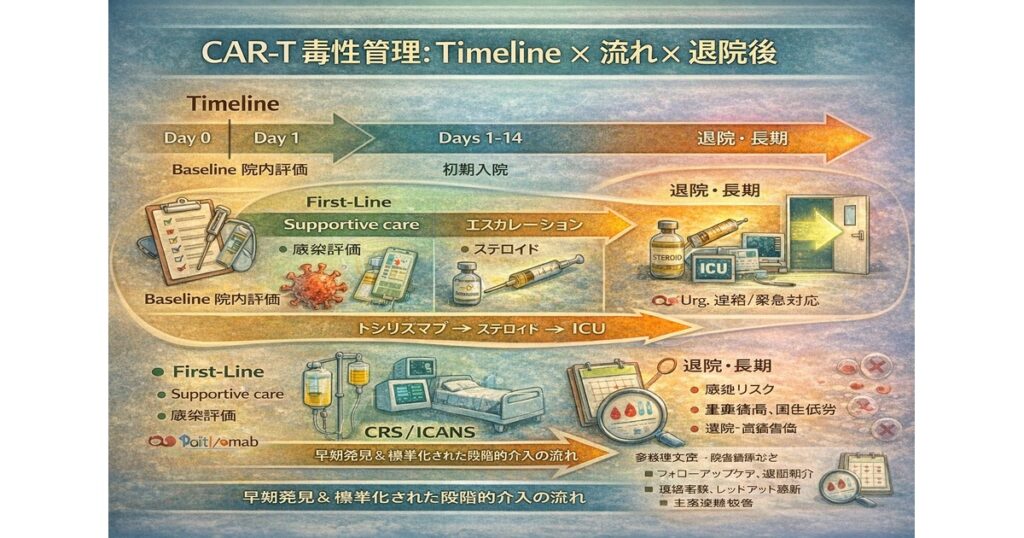
(ここに冒頭図を挿入:Canva 1200×630)
推奨図(英語のみでもOK):“CAR-T Toxicity Management: Timeline × Actions × Follow-up”
- 左:Day 0〜Day 14(CRS/ICANSが多い時期)
- 中:First-line / Escalation(Tocilizumab→Steroids等)
- 右:Discharge & Long-term(感染・血球減少・追跡)
- 下帯:“Early detection & standardized escalation pathways”
まず結論(エグゼクティブ・サマリー)
- CAR-Tの毒性管理は「怖い副作用に耐える」のではなく、**早期検知→標準化された段階的介入(escalation)**でコントロールする設計思想です。
- 現場は概ね ASTCTのCRS/ICANSグレーディングを共通言語にして動きます(多職種連携の前提)。
- 2025年6月、FDAは承認済みBCMA/CD19自家CAR-TのREMSを撤廃しました。これは「リスクはラベル/Medication Guideで十分伝達できる」レベルまで運用が成熟したという評価です。
- 一方で、FDAは2024年4月に **T細胞悪性腫瘍(T-cell malignancies)**のリスクをクラスとして強調し、Boxed Warning等のラベル改訂を求めました。つまり「提供モデルは簡素化しつつ、長期安全性はより厳格に追う」方向です。
- 事業/施設運用の要点は「ICUに行かせない」ではなく、**重症化前に拾い上げる体制(教育・トリアージ・24/7連絡・薬剤在庫・プロトコル)**を作れるかにあります。
1) 毒性管理の“座標系”:何を、いつ、どう見て、どう上げるか
ここを揃えると、施設・企業・論文の話が同じ言葉で読めます。
1-1. いつ起きやすいか(時間軸の理解)
- 早期(多くは投与後〜2週):CRS(発熱・低血圧・低酸素)とICANS(意識/言語/けいれん等)が集中
- 回復期(退院後〜数週〜):感染、血球減少(遷延)、体力低下、再入院トリガー
- 長期:二次性悪性腫瘍(T細胞悪性腫瘍等)の監視、免疫再構築、ワクチン計画
※「2週以内に多い」は一般論で、製品/患者背景でズレますが、運用設計の起点として強いです。
1-2. 何を共通言語にするか(ASTCTの意味)
CRS/ICANSは施設間で表現が揺れると危険なので、ASTCTのスケールが共通言語として機能します。CRSは“発熱+低血圧/低酸素”で重症度を上げ、治療介入後は“発熱がなくても”低血圧/低酸素で評価する点が重要です。
2) CRS(サイトカイン放出症候群):実務としての見方と介入
2-1. 典型像(現場が最初に拾うもの)
- 発熱(最頻)、悪寒、倦怠感
- 進行すると:低血圧(輸液反応性→昇圧薬)、低酸素(酸素投与→高流量→人工呼吸)
- “怖い”のは発熱そのものではなく、循環/呼吸に影響が出始めること
2-2. 介入の骨格(概念:First-line→Escalation)
施設ごとに細部は異なりますが、骨格は似ます:
- First-line:支持療法(輸液、酸素、解熱、感染評価)+必要に応じ IL-6経路阻害(例:トシリズマブ)
- Escalation:持続する低血圧/低酸素、進行例では ステロイド を含む強化、ICU連携
- 重要:**「早めにトシリズマブ」**は“効かせるため”より「重症化前の制御」の意味が大きい(施設プロトコルで一貫性が出る)
2-3. 感染との見分け(実務の罠)
CRSの発熱と感染性発熱は重なります。実務では「どちらか」と割り切らず、感染評価を並走しつつ、CRSを疑うなら介入を遅らせない、が基本姿勢になります。
3) ICANS(神経毒性):家族が気づく“兆候”を医療に落とす
3-1. 典型像
- “言葉が出ない/会話が噛み合わない”
- 混乱、注意障害、強い眠気
- 頭痛、振戦
- 進行例:けいれん、意識障害、脳浮腫(稀だが最重要)
3-2. スクリーニング(ICEスコアの思想)
ICANSは、患者の応答(見当識/命名/追唱など)を使った簡易評価で“数字化”して共有できるのが強みです(臨床現場ではICEスコア)。
3-3. 治療の骨格
- ICANSはトシリズマブ単独で解決しないことがある(CRSと違う点)
- 施設では ステロイド を中心に、けいれんリスクには 抗けいれん薬、重症例はICU/脳波/画像の連携
- 実務で大事なのは「軽い違和感を見逃さない」こと。家族の観察は、**“事実ベースの共有”**として価値が出ます(A2のメッセージを専門運用に接続)。
4) 退院後運用:感染・血球減少・再来院トリアージ
4-1. 退院後リスクは“別の顔”
早期のCRS/ICANSが落ち着いても、退院後は
- 感染(特に発熱)
- 血球減少(遷延)
- 出血/貧血症状
が再受診・再入院の主要因になります。
4-2. 施設運用としての要点
- 24/7の連絡導線(“誰が受けるか”まで決める)
- 「何℃で電話」「どの症状で救急」など 明文化したトリアージ基準
- 抗菌薬/抗ウイルス/抗真菌の方針、ワクチン再開、生活指導のパッケージ化
- 患者/家族が迷わない“1枚紙”の徹底(ここは実務上、最も効果が高い)
5) 施設運用:REMS撤廃後も残る“本質的な要件”
FDAがREMSを撤廃したのは「リスクが消えた」ではなく、「リスク伝達/管理が標準化した」評価です。
したがって、施設が本当に作るべきなのは以下です:
5-1. 人(教育と役割)
- 医師/看護/薬剤/ICU/救急/神経内科の連携
- 夜間休日の判断者、エスカレーションの責任ライン
- “症状を見た人がすぐ上げられる”文化(ヒヤリの拾い上げ)
5-2. モノ(薬剤・検査・搬送)
- トシリズマブ等の確保(在庫・投与フロー)
- ステロイドプロトコル
- 迅速検査(血液、培養、炎症、画像、EEG)
- ICU搬送・転院ルートの確保
5-3. ルール(プロトコル)
- CRS/ICANSの院内グレーディングと介入基準
- 退院後の連絡基準
- 事後レビュー(症例ごとの改善サイクル)
6) 長期安全性:Boxed Warningと「生涯フォロー」の現実
FDAは、BCMA/CD19自家CAR-Tにおいて T細胞悪性腫瘍リスクをクラスとして強調し、Boxed Warning等の改訂を求めました。
ここで重要なのは、“恐怖”ではなく 運用として追うことです:
- 長期フォロー(生涯監視が推奨/要求される文脈が強い)
- 症状がなくても追跡(定期診察・検査)
- 患者説明(なぜ追跡が必要かを納得してもらう)
「REMS撤廃=簡単になった」ではなく、むしろ 急性期管理は標準化、長期安全性の責任は明確化という整理が実務的です。
7) CMC/比較性:毒性“そのもの”ではなく、毒性を左右する基盤
FDAのCAR-T開発ガイダンスは、CMC、非臨床、臨床設計に加え、**分析的比較性(analytical comparability)**の推奨事項を明示しています。
これは「製造変更(スケール、工程、施設変更)」が起きたときに、有効性・毒性・品質が同等であると説明できるかが、事業の継続性を左右するためです。
投資・BD視点では、臨床結果だけでなく「比較性戦略」を読むのが、CAR-Tの目利きになります。
8) 次回の接続(シリーズの流れ)
- A3(一般):固形がんでCAR-Tが難しい理由(3つの壁)
- B3(専門):次世代CAR設計(多標的、論理ゲート、Armored、局所投与、デリバリー)
- A4/B4:自己免疫など“がん以外”への拡張(安全域設計・可逆性)
一次情報(主要ソース)
- FDA:REMS撤廃(Press Release, Jun 2025)
- FDA:T細胞悪性腫瘍に関するBoxed Warning(Apr 2024)
- FDA:CAR-T開発ガイダンス(Mar 2024)
- ASTCT:CRS/ICANSコンセンサスグレーディング(2019)








コメント