A5(一般向け)から読みたい方はこちら:→ A5:in vivo CARとは?「体内でCAR細胞を作る」次世代アプローチ
A5(一般向け)から読みたい方はこちら:
→ A5:in vivo CARとは?「体内でCAR細胞を作る」次世代アプローチ
この記事でわかること
- まず結論(エグゼクティブ・サマリー)
- 1) Delivery(デリバリー):in vivo CARの“本丸”
- 2) Control(制御):in vivo CARの“投与設計”がプロダクトになる
- 3) Safety(安全性):in vivoは“オフターゲット”が主戦場
- 4) CMC/Reg(CMC・規制):in vivoは“薬”としての一貫性が勝負
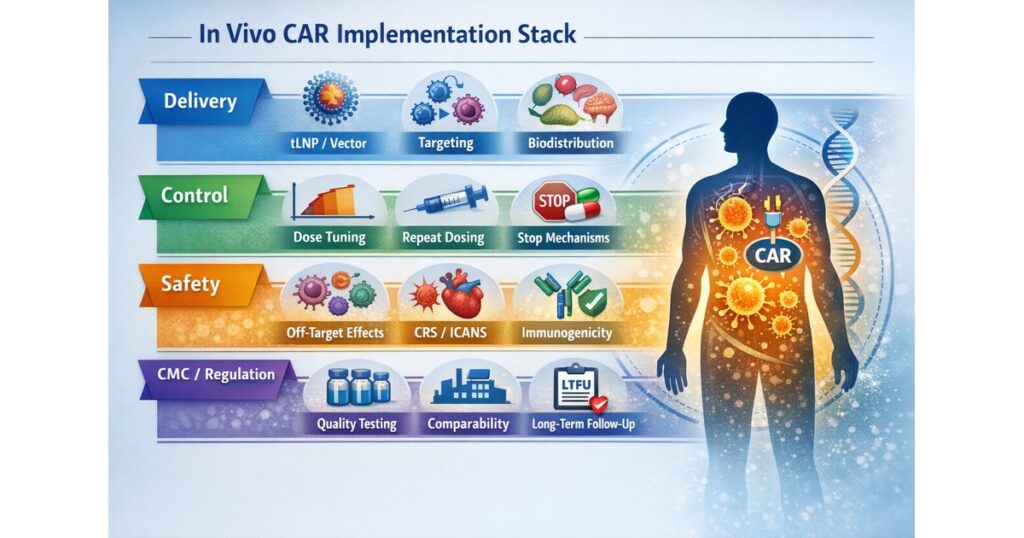
「In vivo CAR Implementation Stack」
- Delivery(tLNP/ベクター、標的化、分布)
- Control(dose-dependent、repeat dosing、停止策)
- Safety(off-target、CRS/ICANS、免疫原性、長期リスク)
- CMC/Reg(規格、放出試験、比較性、LTFU)
まず結論(エグゼクティブ・サマリー)
in vivo CARの本質は「CAR-Tを作る工程を体内に移す」ことではなく、“体内で起きる分布・制御・安全性”を医薬品として再現可能にすることです。勝負どころは以下の4点に集約されます。
- どの細胞に、どれだけ届くか(targeted biodistribution)
- どれだけ強く、どれだけ長く働かせるか(tunable controllability)
- 意図しない細胞・組織で何が起きるか(off-target toxicology)
- 同じ品質を量産・規格化できるか(CMC・放出試験・比較性)
この領域を現実に押し上げたのが、CD8標的tLNPでCAR mRNAをT細胞へ届けるScience論文(2025)と、CapstanのCPTX2309のPhase 1開始発表です。
さらに2025年にはAbbVieがCapstanのin vivo CAR技術を大型買収する動きも報じられ、産業側の確度が一段上がったことを示します。
1) Delivery(デリバリー):in vivo CARの“本丸”
1-1. 何を運ぶか:mRNA(トランジェント) vs DNA/ベクター(長期)
- mRNA(LNP/tLNP):発現が時間で切れる=「止まる」という安全弁。反復投与・用量調整の設計が取りやすい。
- DNA/ベクター:長期発現の可能性がある一方、長期安全性・追跡の要求が重くなりやすい(自己免疫で許容されるかが争点)。
現状の“最も臨床に近い”潮流は、tLNP×mRNA×標的化で「可逆性と制御性」を取る方向です。
1-2. どの細胞に届けるか:CD8標的化が象徴する設計思想
Science(2025)は、特定T細胞サブセットへのtLNP標的化という設計で、in vivoでCAR-Tを作る戦略を提示しました。要点は「静脈投与→肝臓トラップ」の古典問題を、標的化で押し返すことです。
読者が見るべきKPI
- 標的細胞での transfection efficiency(導入効率)
- 標的外細胞(肝・単球・内皮など)での off-target expression
- 血液だけでなく 組織(リンパ節・脾臓・炎症部位) での分布
1-3. “分布”が治療価値を決める:自己免疫 vs がん
- 自己免疫:B細胞/自己抗体ドライバーを狙うなら、リンパ系・炎症局所へ届く設計が価値。
- がん:腫瘍局所へ到達できるかが価値(ここはB3の「到達性」の延長線)。
CapstanのCPTX2309は、CD8+ CAR Tのin vivoエンジニアリングとB細胞デプリーション(血液+組織)、さらにB細胞が“よりナイーブ寄り”に再構築する可能性を非臨床として示した、と説明しています。
2) Control(制御):in vivo CARの“投与設計”がプロダクトになる
2-1. dose-dependent(用量依存)をどう担保するか
Capstanは「tunable and dose-dependent levels of CAR expression」を強調しています。これは自己免疫で特に重要で、強すぎる免疫活性化を避けるための中心概念です。
ここでの論点は「投与量→発現量→効果/毒性」の関係が、
- 個体差(体重、免疫状態)
- 炎症状態(血管透過性、標的細胞量)
でどれだけブレるかです。
2-2. repeat dosing(反復投与)を“できる”にする条件
mRNA/tLNP系の強みは反復投与ですが、成立条件があります:
- LNPや抗体部分への 免疫原性(中和で効かなくなるリスク)
- 投与間隔の最適化(効果と安全のバランス)
- 反復で蓄積する予期せぬ炎症
このあたりは、論文化よりも臨床で“運用パッケージ”として固まっていく部分です。
2-3. “止める”はどう担保されるか
ex vivo CAR-Tでは「安全スイッチ」「薬剤誘導性停止」などが議論されますが、in vivoでは
- 発現が時間で切れる(mRNA)
- 投与を止める
が最も強い停止策になり得ます。逆に、長期発現の方式では停止策の設計要求が跳ね上がります。
3) Safety(安全性):in vivoは“オフターゲット”が主戦場
3-1. on-target毒性(B細胞枯渇)は“副作用ではなく設計”
CD19を狙う場合、B細胞が減ること自体は設計どおりです。問題はその後:
- 感染リスク(免疫低下)
- 免疫再構築の質(戻り方)
- ワクチン・予防投与の設計
CPTX2309は「深いB細胞デプリーション」と「ナイーブ優位の再構築」を非臨床として示唆していますが、臨床での再現性が次の焦点です。
3-2. off-target expression:最重要リスク
もし肝細胞や単球などがCARを発現したら、想定外の毒性が起き得ます。したがって、
- 標的化(例:CD8標的)
- 発現の局在化(必要最小限)
- 発現期間の制御(mRNA)
がセットで問われます。
3-3. CRS/ICANSは“ゼロではない”前提で設計する
in vivoでも免疫が強く動けばCRS/ICANS様の事象は起こり得るため、B2で整理した毒性管理思想(早期検知・段階的介入)は依然として重要です(ただし頻度/形は変わり得る)。
3-4. 長期安全性:遺伝子治療の追跡思想(LTFU)
FDAは遺伝子治療製品の長期フォローアップ(LTFU)ガイダンスを提示しています。in vivo CARが「遺伝子治療/遺伝子改変」の枠組みに入るほど、追跡設計が重くなります。
(mRNAのトランジェント設計が“自己免疫で受け入れやすい”理由の一部はここにあります)
4) CMC/Reg(CMC・規制):in vivoは“薬”としての一貫性が勝負
ex vivo CAR-Tでは「細胞製品の放出試験」が中心でした。in vivoでは、
- LNPの粒径・封入率・純度
- 抗体/リガンドの結合能
- mRNA品質(配列、修飾、キャップ、dsRNA不純物)
- 力価(potency)の定義(“T細胞が何%CAR化し、機能するか”をどう規格化するか)
が核心になります。
特に難しいのは potencyの設計です。
「同じ投与量」でも、患者のT細胞状態が違えばCAR化・増殖・効果が変わる。ここを“製剤の品質”と“患者因子”に分けて説明できるかが、規制・製造・商業化の壁になります。
5) 産業ダイナミクス:AbbVieの大型買収が示すもの
Natureの報道では、AbbVieがCapstanを約21億ドルで買収し、in vivo CAR技術(mRNA-LNPによる免疫細胞再プログラム)にベットしたとされています。
これは「まだ早い研究」から「プラットフォーム投資の対象」へ移った象徴的イベントです。
読者がここから得るべき示唆
- モダリティとしての“勝ち筋”が見え始めた(少なくとも自己免疫)
- ただし勝負は「科学」より「実装(デリバリー×制御×CMC)」へ移る
6) in vivo CARニュースの“プロ評価”チェックリスト(コピペ可)
- 何を届ける?(mRNA vs DNA)
- 標的化は何で担保?(例:CD8標的)
- off-targetはどこまで評価?(肝・単球・内皮・骨髄など)
- dose-dependentが成立している証拠は?
- repeat dosingの障害(免疫原性/中和)は?
- potencyはどう定義?(規格化できそうか)
- LTFU/長期追跡はどう設計?
次回(A6/B6の流れ)
プラン通り次は A6(一般:製造とアクセス—なぜ高い?どう変わる?)→B6(専門:COGS/サプライチェーン/施設要件/規制と商業化) が最も自然に繋がります。
主要参考(一次)
- Science(2025):CD8標的tLNPでin vivo CAR-T生成
- Capstan(2025):CPTX2309 Phase 1開始(dose-dependent CAR expression等)
- FDA(2020):遺伝子治療LTFUガイダンス
- Nature(2025):AbbVieによるCapstan買収報道
編集部より
この記事で取り上げたのは以下の論点です。
- まず結論(エグゼクティブ・サマリー)
- 1) Delivery(デリバリー):in vivo CARの“本丸”
- 2) Control(制御):in vivo CARの“投与設計”がプロダクトになる
- 3) Safety(安全性):in vivoは“オフターゲット”が主戦場
断片的なニュースや用語の紹介ではなく、一つの流れとして読めるように整理しました。同じテーマでもう一歩踏み込みたい方は、関連記事もあわせてお読みください。








コメント