(先にA0を読んでいない方へ)
→ A0:CAR-T療法とは?まず全体像(目次つき)
(固形がんの話から来た方へ)
→ A3:固形がんでCAR-Tが難しい理由(3つの壁)
→ B3:固形がんCAR-Tの突破法(次世代CAR設計)
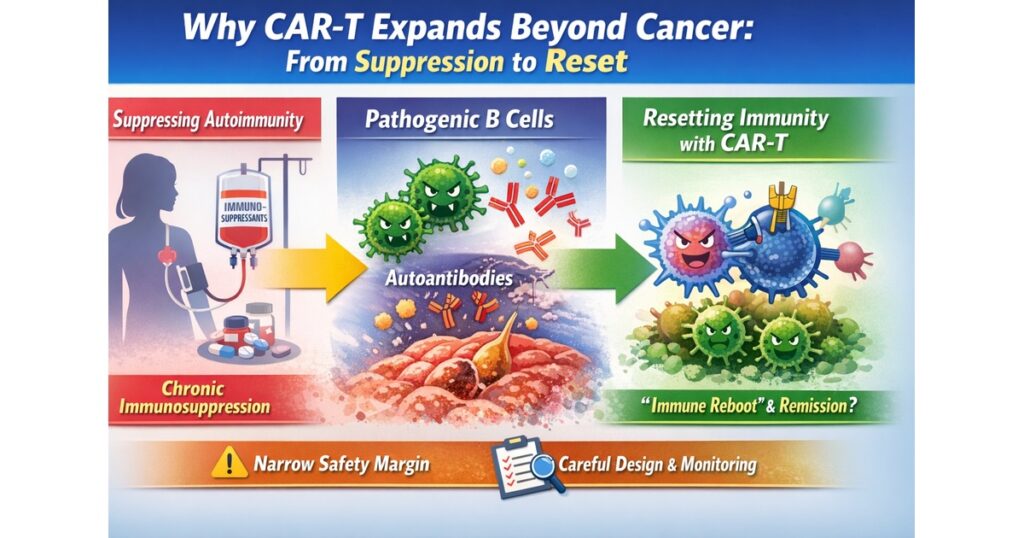
“Why CAR-T Expands Beyond Cancer: From Suppression to Reset”
- 左:従来治療(免疫抑制を継続)
- 中:B細胞/自己抗体のドライバー
- 右:CAR-Tの狙い(病的B細胞の“リセット”→寛解の可能性)
- 下:注意(毒性許容が狭い/設計と運用が重要)
まず結論:自己免疫でCAR-Tが注目されるのは「免疫を抑える」から「免疫を立て直す」へ発想が変わるから
自己免疫疾患(例:全身性エリテマトーデス、ループス腎炎など)は、免疫が誤って自分の体を攻撃し続ける病気です。従来の治療は、多くの場合 免疫を抑える薬を長期で使い続ける発想が中心でした。
ここにCAR-Tが入ってくる理由は、発想が少し違うからです。
CAR-T(特にCD19などを標的にしたタイプ)は、病気を動かしているB細胞(自己抗体を作る側)を大きく減らし、免疫の状態を“作り直す(リセットする)”可能性がある――この点が強烈なインパクトになっています。実際に難治性SLEでCD19 CAR-Tが有望な臨床報告として発表され、注目が一気に広がりました。
1) そもそも「自己免疫」では何が起きている?(やさしい全体像)
自己免疫疾患は一言で言っても多様ですが、共通して起きやすいのは次の構造です。
- 免疫が「外敵」ではなく「自分」を標的にしてしまう
- 炎症が長引き、臓器(腎臓・皮膚・関節・神経など)に障害が出る
- 病気が落ち着いても、再燃(ぶり返し)が起こり得る
- 治療は長期になりやすく、感染症などの副作用とも付き合う必要がある
この「慢性化・再燃・長期治療」の構造が、次の“CAR-Tの発想”につながります。
2) なぜB細胞が鍵になりやすい?(CD19が出てくる理由)
自己免疫の多くで、B細胞は重要な役割を持ちます。
- 自己抗体(自分を攻撃する抗体)に関わる
- 免疫のスイッチを入れたり、炎症を持続させたりする
- 他の免疫細胞の動きを助長することがある
だから、B細胞を標的にする治療(例:抗CD20抗体など)は、自己免疫でもすでに一般的です。
CAR-Tはこの延長線上にありつつ、**「より深くB細胞を減らし、免疫の再構築を促す」**という点で“次の段階”として見られています。
3) 「免疫を抑える治療」と「免疫を立て直す治療」の違い
ここがA4の核心です。
従来:免疫を抑える(Suppression)
- 病気の火を小さくする
- ただし、やめると再燃しやすいことがある
- 長期免疫抑制に伴う感染リスクなどが課題になることがある
CAR-Tの狙い:免疫を立て直す(Reset / Reboot)
- 病的な免疫回路を“作り直す”方向性
- 理想的には、薬をずっと続けなくても長期寛解に近づく可能性
- ただし、実現には安全性・設計・運用の壁がある
難治性SLEでのCD19 CAR-T報告では、治療後にB細胞が戻ってくる際に“よりナイーブ寄り”の再構築が示唆され、免疫の再編という発想を後押ししました。
4) どんな自己免疫で開発が進む?(A4は大分類だけ)
現時点で注目されやすいのは、ざっくり以下のカテゴリです(病名の細かい話はB4で深掘りします)。
4-1. 自己抗体が強く関わる疾患(代表:SLE/ループス腎炎など)
自己抗体が病勢に関わるタイプは、B細胞標的の理屈が通りやすく、CAR-Tの議論が先行しています。
企業開発も進み、たとえばKyvernaはB細胞駆動型自己免疫向けにCD19 CAR-T(KYV-101)を開発し、ループス腎炎で試験が進められています。
4-2. 線維化・臓器障害が強いタイプ(例:強皮症など)
自己免疫の中でも臓器障害が問題になる領域は、長期予後の改善が大きな価値になります。研究報告・レビューが増えてきています(ここはB4で体系化します)。
4-3. 神経・筋の自己免疫(例:重症筋無力症など)
免疫の誤作動が神経筋接合部などに影響する領域でも、B細胞ドライバーがある場合に議論対象になります(B4で扱います)。
5) ここが“がん領域と違う”:自己免疫CAR-Tは毒性許容が狭い
がん領域では「難治がんに対してベネフィットが大きい」ため、一定の毒性を許容してでも攻める設計が成立します。
一方、自己免疫では、患者さんの背景や病勢にもよりますが、一般に 毒性の許容範囲が狭い。
だから自己免疫CAR-Tは、次の方向に設計思想が寄ります:
- より免疫原性の低い構成(例:fully human CARの志向)
- できるだけ安全域を広くする(“強すぎない・暴走させない”)
- 長期フォローアップ設計が前提(遺伝子改変治療としての追跡)
6) 「一回で治る」のか?—期待と現実を分ける
ここは誤解が最も増えるので、先回りします。
- 期待できる点:免疫の再構築が起きれば、長期寛解に近づく可能性がある(初期報告が注目を集めた理由)。
- 現実的な注意:症例数はまだ限定的で、疾患ごとに最適条件(前処置、投与量、モニタリング)は確立途上。レビューでも「解くべき論点」が整理されています。
7) 退院後・長期フォローの考え方(家族が安心するポイント)
CAR-Tは遺伝子改変細胞治療の文脈を持つため、長期フォローアップの考え方が重要です。FDAは遺伝子治療製品の長期追跡(LTFU)に関するガイダンスを出しており、自己免疫CAR-Tでも「長期で追う」設計が基本になります。
患者さん・家族の実務としては、
- 退院後の連絡基準(発熱、意識、感染兆候)
- 定期検査の意味(免疫の回復、感染、長期安全性)
を「決めておく」ことが不安を減らします。
FAQ(検索で多い質問)
Q1. 自己免疫にCAR-Tはもう使えるの?
原則として多くは臨床試験段階です。ただし、難治例での報告が注目され、企業試験も進んでいます。
Q2. どうしてCD19がよく出てくるの?
B細胞を狙うための代表的標的だからです。自己免疫でB細胞が病勢に関わる場合、理屈が通りやすい。
Q3. がんのCAR-Tより安全なの?
一概に言えません。自己免疫は毒性許容が狭いので設計・運用はより慎重になります。長期フォローも前提です。
次回予告(B4)
次回の **B4(専門向け)**では、自己免疫CAR-Tを
- 疾患カテゴリ別(SLE/LN、強皮症、神経系など)
- 設計思想別(B細胞デプリーション、可逆性、fully human、前処置の設計)
- 企業・プログラム別(代表例)
で「読める形」に整理します。
参考(一次・総説)
- 難治性SLEに対するCD19 CAR-T報告(Nature Medicine, 2022)
- 自己免疫におけるCAR-Tの総説(Frontiers in Immunology, 2025)
- ループス腎炎でのKYV-101試験情報(Kyverna/ClinicalTrials.gov)
- FDA 遺伝子治療の長期フォローアップ(LTFU)ガイダンス(2020)
コメント