(先にA0を読んでいない方へ)
→ A0:CAR-T療法とは?まず全体像(目次つき)
(自己免疫の流れから来た方へ)
→ A4:CAR-Tが「がん以外」に広がる理由(免疫リセット)
→ B4:自己免疫CAR-Tの最前線(設計思想・企業動向)
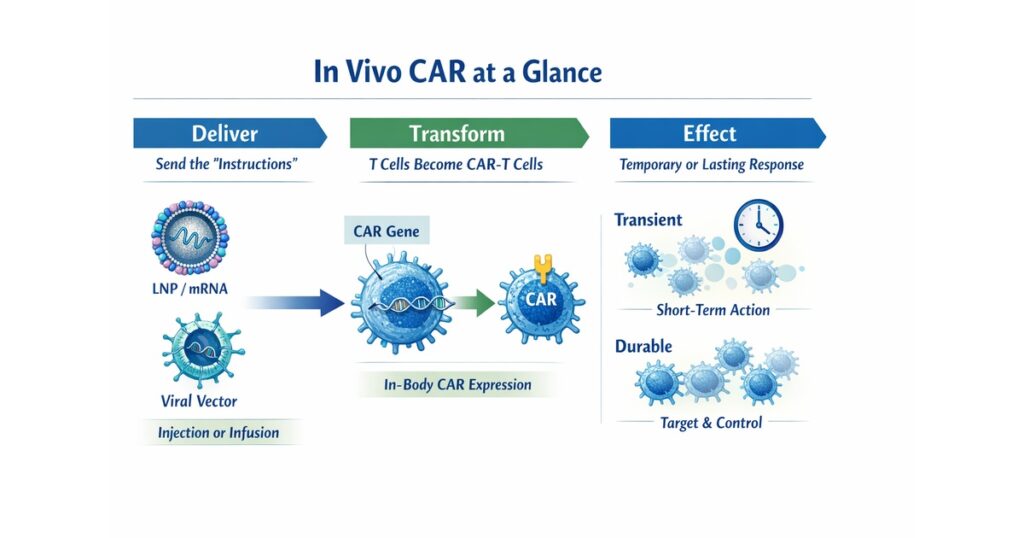
「In vivo CAR の全体像:投与 → 体内でT細胞をCAR化 → 一時的/持続的に働く」
図の3ブロック:
- 何を投与する?(LNP/mRNA、ウイルスベクター等)
- 体内で何が起きる?(標的細胞に遺伝子が届く → CAR発現)
- 何が嬉しい?何が難しい?(アクセス/コスト vs 安全性/制御)
まず結論:in vivo CARは「体外で作るCAR-T」を“体内で作る”発想
これまでのCAR-Tは、患者さんのT細胞を採取して、体の外(ex vivo)でCARを導入して増やし、戻す——という工程が必要でした。
一方 in vivo CAR は、体内に“設計図”を届けて、患者さんの体の中でCAR細胞を作ることを狙います。
イメージはこうです:
- 従来CAR-T:工場(体外)で作ってから輸送(投与)
- in vivo CAR:体内に設計図を届け、現場で製造(体内でCAR化)
この発想が注目される理由は、もし成立すれば「時間」「コスト」「施設要件」の壁を一気に下げられる可能性があるからです。
1) なぜin vivo CARが必要?—「CAR-Tのボトルネック」を外すため
従来のCAR-T(体外製造)には、一般の人にも分かりやすい“壁”があります。
- 細胞採取・製造・輸送に時間がかかる(待機期間が生じる)
- 製造できる施設と運用ノウハウが必要
- コストが高く、アクセスが限られやすい
- 個別製造(患者ごと)なのでスケールしにくい
in vivo CARは、この“ボトルネック”を「投与型」に近づけて、より多くの患者さんに届く治療にするという動機で進んでいます。
2) どうやって体内でCAR細胞を作るの?(超ざっくり3パターン)
in vivo CARは、何を体内に届けるかで大枠が分かれます。
パターンA:mRNAを届ける(LNPなど)=「一時的にCARを出す」発想
- 体内の標的細胞にmRNAを届ける
- 一定期間だけCARが発現して働く
- 作用が切れる=安全性と制御の面で利点になり得る
この方向性は、近年のレビューや解説でも「臨床に持ち込みやすい実装」として重要視されています。
パターンB:DNAを届ける(ウイルスベクター等)=「長くCARを出す」発想
- 遺伝子として届けることで、より長く発現し得る
- ただし、長期発現は長期安全性の設計がより重要になる
パターンC:体内で遺伝子編集/組込みを起こす(将来的な拡張)
- 精密に「特定細胞だけ」を狙う必要があり、実装難易度は高い
- ただし成功すれば“真のin vivo細胞治療”になる可能性がある
A5では全体像までに留め、B5でデリバリー/制御/安全性/規制を深掘りします。
3) 「いまどこまで来ている?」—学術と企業で動きが具体化
in vivo CARは「夢」ではなく、学術・産業の両方で“具体の形”が見えています。
3-1) 学術(概念実証):CD8標的LNPでin vivo CARを作る報告
Science(2025)では、CD8標的LNPで抗CD19 CAR mRNAを届け、体内でCAR-Tを作るという報告が出ています(がんと自己免疫の両方を意識した内容)。
ここでの重要点は「狙った細胞に届ける(targeted)」ことと、「mRNAで可逆性(トランジェント)を持たせる」思想です。
3-2) 企業(臨床へ):Capstan Therapeutics(CPTX2309)
Capstanは、tLNP(targeted LNP)を使い anti-CD19 CAR mRNAをT細胞へ届けるin vivo CAR-T(CPTX2309)で、自己免疫(B細胞駆動)を対象にPhase 1開始を公表しています。
この手の設計は「投与でCAR発現量を調整できる(tunable/dose-dependent)」ことが強調されがちで、自己免疫領域の“毒性許容が狭い”条件にフィットし得ます。
4) in vivo CARのメリット(読者が押さえるべき“期待できる点”)
A5では、誇張せず、しかし構造的メリットを整理します。
- 速い:採取・製造・輸送の待機を減らせる可能性
- 広がる:高度施設依存を下げ、アクセスを広げ得る
- 繰り返せる可能性:mRNA型なら“必要に応じて追加投与”という設計が取りやすい
- コスト構造の改善余地:個別製造から“投与型”へ近づくほど改善余地が出る
5) ただし課題も明確:in vivo CARの「3つのリスク」
in vivo CARは便利そうに見えますが、課題ははっきりしています。ここを理解するとニュースが読めます。
リスク①:どの細胞に届くか(標的外デリバリー)
“狙ったT細胞だけ”に届けるのが難しいと、意図しない細胞がCARを出してしまう可能性があり、リスクになります。
だからこそ targeted delivery(例:CD8標的LNP)が重要になります。
リスク②:強さをどう制御するか(暴走をどう止めるか)
CARが強すぎると毒性が問題になります。
mRNA型の利点は“時間で切れる”ことですが、それでも投与量・投与間隔・反応性の個体差をどう扱うかが鍵です。
リスク③:長期安全性と追跡(規制上の前提)
in vivo CARも遺伝子治療/遺伝子改変の文脈を持ち得るため、長期追跡(LTFU)の考え方が重要になります。FDAは遺伝子治療のLTFUガイダンスを公開しています。
6) どう読む?in vivo CARニュースの「4点チェック」
今後ニュースが増えるので、読み方を固定します。
- 何を届ける?(mRNA/LNP か、DNA/ベクターか)
- どの細胞へ?(CD8など標的化の仕組みは?)
- 可逆性は?(一時的か、長期か)
- 安全性の作り方は?(投与量制御、停止策、追跡設計)
次回予告(B5)
B5(専門向け)では、in vivo CARを「実装論点」で解剖します:
- デリバリー(LNP設計・標的化・分布)
- 制御(tunable、repeat dosing、停止策)
- 安全性(毒性、免疫原性、オフターゲット)
- 規制・CMC(品質、再現性、LTFU)
コメント