まず全体像(A4)から読みたい方はこちら:
→ A4:CAR-Tが「がん以外」に広がる理由(自己免疫は“免疫のリセット”という発想)
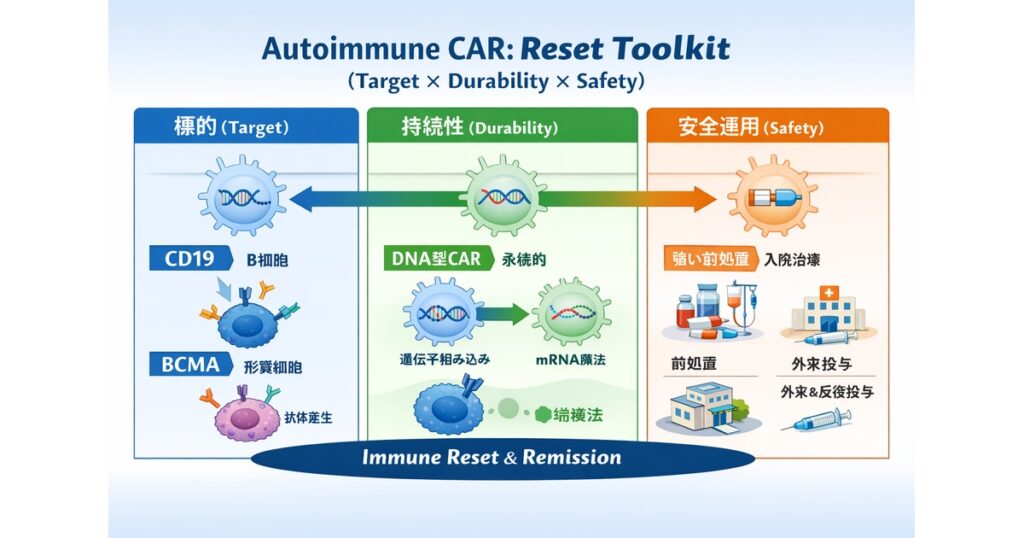
“Autoimmune CAR: Reset Toolkit (Target × Durability × Safety)”
- Target axis:CD19(B cells)↔ BCMA(plasma cells)
- Durability axis:DNA-integrating CAR ↔ transient mRNA CAR
- Safety axis:conditioning強 ↔ conditioning無し/軽い など
まず結論(エグゼクティブ・サマリー)
自己免疫CAR-Tは、がん領域の「腫瘍細胞を叩く」から、免疫回路を“リセット”して寛解を狙うへ重心が移ります。そのため設計と運用の最適化ポイントも変わります。
- 標的の中心はCD19(B細胞)。難治性SLEでのCD19 CAR-T報告が“免疫リセット”という物語を強く後押ししました(A4の根拠)。
- 臨床開発の主流は **「CD19 CAR-T(fully human志向、4-1BB共刺激の系譜)」**で、Kyverna(KYV-101)やCabaletta(CABA-201)などが代表例として挙げられます。
- 一方、**BCMA(形質細胞)を狙う“mRNA CAR-T”**という別解があり、Cartesian TherapeuticsのDescartes-08は「外来・前処置なし・反復投与」という設計思想でMG(重症筋無力症)領域を進めています。
- 遺伝子改変細胞治療として、**長期フォローアップ(LTFU)**は“標準の設計要件”。FDAのLTFUガイダンスが枠組みを示しています。
1) 自己免疫CAR-Tの「座標系」:標的 × 持続性 × 安全運用
自己免疫は毒性許容が狭い(A4のポイント)ので、ここを座標系として読むと理解が早いです。
1-1. 標的(Target)
- CD19:B細胞を広くカバー(自己抗体ドライバーの上流を叩く発想)
- BCMA:形質細胞(抗体産生の“現場”)に寄せる発想(とくに神経筋疾患などで議論)
1-2. 持続性(Durability)
- 従来型CAR-T(遺伝子改変で持続):深いデプリーション→免疫再構築(reset)を狙う
- mRNA CAR-T(トランジェント):短い作用を積み上げ、安全域と外来運用を優先(Descartes-08が代表)
1-3. 安全運用(Safety & Operations)
- conditioning(前処置)の強さ、入院/外来、モニタリング設計が価値そのもの
- LTFU(長期追跡)は「やるかどうか」ではなく「どう設計するか」
2) 疾患カテゴリ別:どこで現実味が高いか(B4は代表まで)
自己免疫CAR-Tは「全部に効く」という話ではなく、ドライバーの構造で適合度が変わります。
2-1. 自己抗体・B細胞ドライバーが強い領域(SLE/LNなど)
- 難治性SLEでのCD19 CAR-T報告が、免疫リセットの臨床像を提示し、以後の産業開発の地図を作りました。
- KyvernaはKYV-101(fully human CD19 CAR-T)をB細胞駆動型自己免疫で開発し、**ループス腎炎(LN)**での試験情報を公開しています(ClinicalTrials.govにも記載)。
この領域の“勝ち筋”
- ①深いB細胞デプリーション → ②再構築(naïve寄りの回復) → ③薬剤依存の低下
ただし、患者選別(病勢・臓器障害・既治療)と安全運用設計が成否を分けます。
2-2. 炎症性筋疾患・全身性疾患(myositis / systemic sclerosis 等)
CabalettaはCABA-201(fully human, 4-1BB, CD19 CAR-T)を「重症自己免疫」向けに整理しており、SLE/筋炎/強皮症などを含む文脈を示しています。
この領域の“読みどころ”
- “リセット”が臓器障害の長期予後に効くか
- 評価指標が腫瘍と違い複雑(症状・機能・バイオマーカー・ステロイド削減など)
2-3. 神経免疫(重症筋無力症:MG など)
Cartesian TherapeuticsのDescartes-08は、BCMA指向のmRNA CAR-TとしてMGを対象に臨床が進み、外来・前処置なし・反復投与という設計思想が特徴として語られています。
この領域の“勝ち筋”
- 形質細胞/抗体産生に寄せた標的選択(BCMA)
- トランジェント設計で安全域と運用性を取りに行く
3) 設計思想別:何が“がんCAR-T”と違うのか
自己免疫では「効く」より先に「安全に回せる」ことが価値になります。ここが腫瘍領域と最大の差です。
3-1. fully human binder(免疫原性の低減志向)
自己免疫は患者の治療期間が長く、再治療・追跡も長い。したがって、免疫原性・再投与可能性への配慮が強く出ます。
Kyverna(KYV-101)やCabaletta(CABA-201)は“fully human”を強調しています。
3-2. 4-1BB共刺激の系譜(持続性と毒性のバランス)
CD19 CAR-Tでも共刺激の違いが議論になります。自己免疫では、持続性を保ちつつ毒性を抑えるバランスが中心テーマです(B5以降の発展テーマにも接続)。
3-3. Conditioning(前処置)をどう設計するか
がん領域の“標準”をそのまま適用できないケースがあるため、
- どの強度が必要か
- conditioning無し/軽い設計は成立するか
が競争点になります(Descartes-08は“without preconditioning”を特徴として語られます)。
3-4. トランジェントCAR(mRNA)という別解
「長期持続=良い」と限らないのが自己免疫の面白さです。
mRNA CARは、
- 作用が切れる(安全域)
- 外来で反復投与できる(運用性)
を武器にします。
4) 規制・安全性:LTFU(長期追跡)は“前提条件”
遺伝子治療・遺伝子改変細胞治療の文脈では、遅発性有害事象を拾うためのLTFUが重要です。FDAはLTFUガイダンスを公開しており、設計の骨格として参照されます。
実務的含意(読者が知っておくべきこと)
- 「治療して終わり」ではなく、追跡が治療パッケージの一部
- “効いた”だけでは開発は進まず、追跡設計・運用コストが勝負になる
- 自己免疫は患者数が多くなり得るため、LTFUを含む運用設計がスケール障壁にもなる
5) 12–24か月で追うべき触媒(Catalysts)
- CD19 CAR-Tの自己免疫領域で、**疾患横断(SLE/LN/筋炎/強皮症)**の再現性が出るか
- “免疫リセット”が、薬剤フリー寛解としてどれだけ維持されるか(追跡期間の伸び)
- mRNA CAR-T(BCMAなど)の外来運用モデルが、治療の標準化に耐えるか
- conditioning強度の最適化(安全性×効果のトレードオフが見えてくるか)
まとめ(B4の要点)
- 自己免疫CAR-Tは「がんの転用」ではなく、免疫回路を再構築する医療として設計される
- 中核は CD19(B細胞)。代表的産業プレイヤーとして Kyverna(KYV-101)、**Cabaletta(CABA-201)**が象徴的
- 別解として **BCMA×mRNA CAR-T(Descartes-08)**があり、外来・前処置なし・反復投与という運用モデルを提示している
- LTFU(長期追跡)は前提条件で、開発とスケールの“見落としがちな本丸”
主要参考(一次・公式)
- Kyverna:KYV-101(LN試験・Fast Track等)
- Cabaletta:CABA-201 pipeline / RESET関連
- Cartesian:Descartes-08(開発状況・特徴)
- FDA:LTFU Guidance(2020)
コメント