A5・B5では、in vivo CAR-T という次世代の実装候補が、単なる新奇な技術ではなく、製造・物流・アクセスの構造問題に対する回答として浮上していることを見てきました。A6ではその流れを患者目線に引き寄せ、CAR-Tがなぜ高く、なぜ届きにくいのかを整理しました。では、より専門的な視点から見たとき、CAR-T商業化の本当の勝負はどこにあるのでしょうか。結論から言えば、それは「強い細胞を作れるか」だけではありません。再現性ある製造を、許容可能なコストで、許容可能な時間で、許容可能な施設負荷のもとに回せるかです。CAR-Tの商業化は、製品開発であると同時に、オペレーティングシステムの設計競争でもあります。
この構造問題を市場が強く意識し始めたことは、ここ1年弱の大型案件からも読み取れます。2025年には AbbVie が Capstan を買収し、同年には Kite が Interius を獲得、さらに 2026年2月には Eli Lilly が Orna Therapeutics を買収しました。いずれも in vivo CAR-T または in vivo cell engineering を含む案件であり、大手が「患者ごと製造・長いTAT・限られた実施施設」という旧来のボトルネックを真正面から再設計しにきていることを示します。つまり現在の競争軸は、単なる有効性の上乗せではなく、COGS、TAT、capacity、QC/CMC、導入施設負荷、価格償還まで含めた総合実装力に移っています。
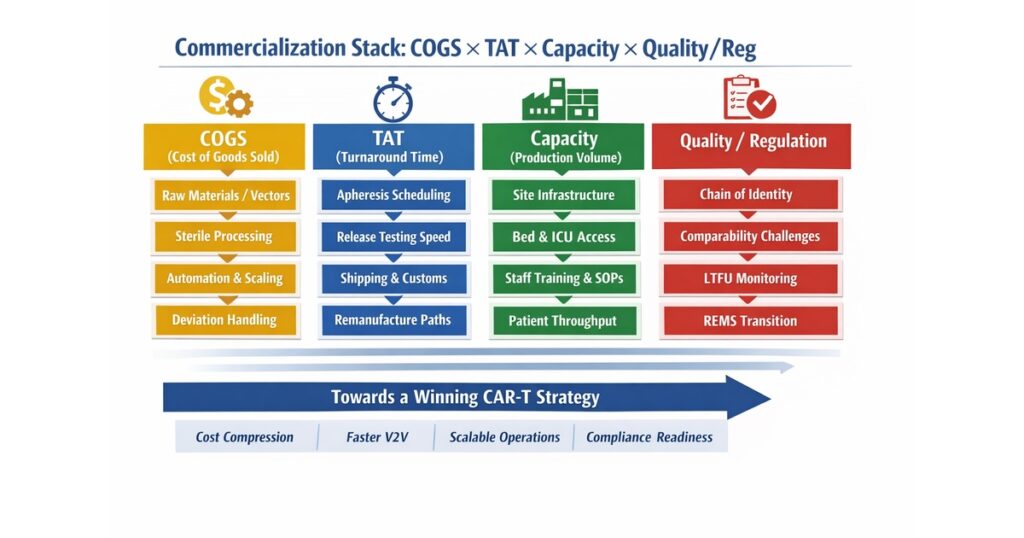
CAR-T商業化で最初に見るべき指標は売上ではなく「システム摩擦」
CAR-Tは高薬価の製品として議論されがちですが、実際には価格の背景にあるのは単一の要素ではありません。
真の問題は、患者由来材料の回収、製造、試験、輸送、投与、急性期管理、長期追跡が、一本の時間制約付きチェーンとして連結されていることです。どこか1か所でも詰まると、他工程の最適化だけでは十分な改善になりません。したがって商業化評価では、売上や薬価を見る前に、まず「そのプラットフォームはどこで摩擦を起こすか」を分解する必要があります。たとえば、apheresisのタイミング、bridging治療の必要性、製造の失敗率、再製造率、release試験のボトルネック、輸送時の保管モード、投与施設のベッド・ICUバックアップ、さらにフォローアップ期間の運用負荷が相互に絡みます。
この観点では、CAR-Tの競争優位は「1回投与で強い奏効を示した」だけでは成立しません。むしろ、いかに多くの適格患者を実際にinfusionまで到達させられるか、その変換効率こそが商業価値を左右します。実臨床データでも、vein-to-vein time(V2Vt)が延びるほど成績や有害事象プロファイルへの影響が無視できないことが示されており、単なる製造KPIではなく臨床KPIとして扱うべき段階に入っています。
COGSは「細胞を作る費用」ではなく、「失敗できない個別製造の総コスト」
専門的にCAR-Tのコストを考えるとき、まず誤解しやすいのはCOGSを培養工程だけで捉えてしまうことです。
実際のCOGSは、原材料、ベクター、無菌製造、人件費、cleanroom/装置、QC試験、逸脱対応、物流、在庫・予約管理、再製造リスク、製造拠点維持費まで含めた総コストです。さらに自家型では、患者単位ロットであること自体が構造的に高コストです。大量生産で平均化できる世界ではなく、患者間ばらつきに由来する品質差や工程差を抱えたまま、毎回GMP的に成立させなければならないからです。
原材料では、依然としてウイルスベクター関連コストが重い要素です。遺伝子導入方式や工程設計によって差は出ますが、ベクターの調達・品質・供給安定性はCOGSだけでなくcapacityにも直結します。非ウイルス法、短縮培養、工程簡素化はコスト低減の有力な方向であり、2025年のレビューでも universal CAR-T、短いexpansion、decentralized manufacturing などが民主化戦略として位置づけられています。
一方で、単純な安価化は品質リスクとトレードオフになりやすい。CAR発現量、細胞生存率、サブセット構成、残留不純物、微生物、複製可能ウイルス関連の確認など、release前に担保すべき項目は多く、試験時間の短縮だけを先行させると安全性またはcomparabilityの問題が前面化します。したがって、B6の文脈でいう「COGS削減」とは、安い工程へ置き換えることではなく、品質設計を壊さずに、どこを標準化・自動化・省工程化できるかという設計問題です。
自動化の本質は省人化ではなく「ばらつき圧縮」
CAR-T製造における自動化は、しばしば人件費削減として語られます。しかし実際の価値は、むしろ工程間・サイト間・オペレーター間のばらつきを圧縮することにあります。2025年のFrontiers論文では、自動化度の高い製造モダリティが、空間効率やcleanroom要件、人件費の面でコスト低減ポテンシャルを持つことが示されました。これは単なる工場効率の話ではなく、商業スケールで「読める工程」を作るための前提です。
CAR-Tでは、同じプロセスを流しても患者材料の状態が異なるため、完全な均質化は困難です。それでも、閉鎖系、自動化装置、デジタル追跡、電子バッチレコード、工程内モニタリングの整備によって、逸脱発生率や手作業依存を減らすことはできます。商業化の観点では、1回の成功バッチよりも、何百例を同じ規律で流せるかの方が重要です。ここで自動化は、COGS改善と同時に規制対応力の改善でもあります。
TATとV2Vは商業指標である前に臨床指標
CAR-Tの供給網で最重要KPIの一つがturnaround time(TAT)であり、その臨床実装上の表現がV2Vです。
なぜ重要かといえば、遅いTATは単に売上回転を悪くするだけでなく、患者が治療へ到達できる確率そのものを下げるからです。axi-celに関する2025年の解析では、V2Vtが長い群で血小板減少の長期化などが増える傾向が示され、早いinfusionの意義が改めて支持されました。別の実臨床報告でも、2L LBCLでのV2Vは試験時より長くなりやすく、現場の混雑やbridgingの影響が露呈しています。
このため、商業化評価で「製造能力あり」とは、単に年間何バッチ流せるかでは不十分です。
見るべきは、
- apheresis予約から製造開始までの待ち
- 製造スロットの柔軟性
- release試験の所要時間
- 国際物流の通関・温度逸脱リスク
- 再製造時のバックアップ導線
- 施設側のベッド・薬剤・スタッフ確保
を含めた総合TATです。
とくにCD19/BCMA領域のように患者状態の悪化が速い適応では、製品スペックが少し上でも、TAT負けするプラットフォームは商業的に不利になります。
サプライチェーンは「温度管理」ではなく「identity管理」の問題
細胞療法の物流は、一般医薬品のコールドチェーンとは本質的に異なります。
CAR-Tでは「冷やして運ぶ」こと以上に、その細胞が誰の細胞で、どの工程を通り、どの条件で保管され、どの患者へ戻るかを一貫して証明し続ける必要があります。chain of identity と chain of custody は、品質問題であると同時に法的・規制的問題でもあります。
このため、サプライチェーン設計では以下が極めて重要になります。
第一に、採取施設・製造施設・投与施設間でデータが切れないこと。
第二に、輸送モード変更や保管形態変更がcomparabilityや安定性評価にどう響くかを把握していること。
第三に、国境をまたぐ場合、通関や搬送会社の実力差まで含めてスケジュール変動を織り込むことです。
細胞そのものは優れていても、identity管理が粗いプラットフォームは商業化しづらい。これは今後 in vivo CAR-T や point-of-care 製造が伸びたとしても消えない視点です。むしろ分散型になれば、IT/追跡・データ整合性の重要性はさらに増します。
Release試験は見落とされがちな「隠れた商業ボトルネック」
多くの議論は製造そのものに集中しますが、実務上はrelease試験が全体TATを押し延ばすことが少なくありません。
無菌性、同一性、活性、細胞数、viability、遺伝子導入関連項目など、何をロット放出に必須とし、何を追加的または事後評価に置くかは、プラットフォーム設計そのものです。2025年のBone Marrow Transplantationの論考や学術製造ユニットのQC harmonization提言でも、release criteriaの整理・標準化が重要なテーマとして浮上しています。
ここでの勝ち筋は、単純な試験削減ではありません。
むしろ、どの属性が本当に臨床的に重要なCQA(critical quality attributes)かを整理し、その評価を早く・再現よく・サイト横断で実施できる体制を作ることです。今後マイクロ流体デバイスなどtime-to-resultを縮める解析技術も注目されますが、それが規制上・実務上どこまで受け入れられるかは慎重な検証が必要です。
Comparabilityは商業スケール移行時の最大の地雷の一つ
CAR-Tの初期開発では、まず患者で動くことが優先されます。しかし商業化段階に入ると、工程変更、装置更新、サイト追加、原材料変更、凍結条件変更、分析法更新などが避けられません。このとき最大の論点になるのがcomparabilityです。
化学合成医薬のように規格値で割り切りにくく、細胞製品は多面的な属性を持つため、「同じ製品」とみなしてよいかの説明が難しいのです。FDAのCMCガイダンス群はこの領域で依然として重要な基盤であり、開発初期から comparability を見据えた分析・保管・変更管理が求められます。
商業化上の教訓は明快です。
初期データを急ぐあまり、後で変更に耐えないプロセスを組むと、上市や拠点拡大で大きく失速します。逆にいえば、B6でいう勝ち筋とは、最初から将来のscale-out/scale-up、分析法の橋渡し、複数拠点管理を想定した「変えても壊れにくいプロセス」を持つことです。これは短期的には遅く見えても、長期の商業価値ではむしろ有利です。
規制の変化:REMS撤廃は「緩和」ではなく「成熟した運用への移行」
2025年6月、FDAはCD19およびBCMA指向の自家CAR-Tについて、CRSと神経毒性に関するREMSを撤廃しました。FDAは、Boxed Warningとラベリング、Medication Guide、そして既存の医療現場経験で安全使用を担保できると判断しています。これは大きな変化ですが、誤解してはいけないのは、安全管理そのものが不要になったわけではないという点です。
むしろこの変化は、CAR-Tが「特別な閉鎖運用」から「高度だが標準化可能な運用」へ移りつつあることを意味します。
施設側には依然として、CRS/ICANSの識別・初期対応、トシリズマブ等の準備、神経学的評価、連携体制、患者教育が求められます。たとえばCARVYKTIの最新ラベルでも、infusion後少なくとも7日間の毎日評価と、少なくとも2週間は医療機関近傍にとどまる指示が維持されています。AUCATZYLでは監視頻度や期間の見直しもみられますが、それは「個別製品の運用最適化」であって、運用負荷ゼロ化ではありません。
したがって商業化の論点としては、REMS撤廃を「市場拡大チャンス」とだけ見るのでは不十分です。正しくは、施設教育・標準手順・地域連携をどう再設計すると、品質を落とさず導入施設を増やせるかという問いに置き換えるべきです。
LTFUは依然として細胞・遺伝子治療の重い宿題
CAR-T、とくに遺伝子改変を伴うプラットフォームでは、長期フォローアップ(LTFU)が依然として重要です。FDAの2020年ガイダンスは、human gene therapy product 投与後の長期追跡の考え方を示しており、長く残る効果や遅発性リスクを前提に観察設計を求めています。さらに2025年には、cell and gene therapy product の postapproval safety/efficacy data capture に関する draft guidance も出され、承認後データ取得の方法論整備が進んでいます。
商業化の観点からLTFUが重いのは、単に規制負担だからではありません。
患者追跡の継続性、データ品質、転院・転居対応、EHRとの接続、registry連携など、上市後オペレーション全体にコストと複雑性を持ち込むからです。特に in vivo CAR-T や integrating platform は、長期追跡に対する市場の視線がより厳しくなる可能性があります。したがって次世代CAR-T企業の価値評価では、臨床データだけでなく、承認後に追跡を回し切る体制があるかも見る必要があります。
施設要件は商業化の見えないCapEx
投与施設の問題は、しばしば販売チャネルの問題に矮小化されますが、実際には人的・物的CapExに近いものです。
経験ある医師・看護師・薬剤師・コーディネーター、緊急時対応、病床確保、近隣患者滞在導線、夜間対応、他科連携まで含めると、CAR-T導入は製品採用というより制度導入です。このため、製品側が扱いやすくなること—TAT短縮、毒性マネジメントの予測可能性向上、投与後拘束期間短縮、モニタリング簡素化—は、そのまま施設拡大可能性につながります。
欧州の2026年マップ研究でも、商業CAR-Tへのアクセス制限要因として、コストと物流複雑性に加え、医療資源不足と償還プロセスが挙げられています。つまり製品が承認されても、それだけで自動的に患者へ届くわけではなく、病院側の実装余力が別のボトルネックとして残るのです。ここに対する一つの回答が、point-of-care製造や地域分散型モデルです。real-world報告では、院内製造型モデルが約3万ドル水準という、欧米上市品の6〜8%程度のコストで機能した例も出てきています。もちろん直接比較には注意が必要ですが、少なくとも「中央集約型しか商業化できない」という前提は揺らぎ始めています。
価格とアクセス:薬価論ではなく「支払いモデル設計」
CAR-Tの価格問題は、しばしば高すぎる薬価として語られます。しかし payer 視点では、問題は価格だけでなく、長期ベネフィットの不確実性をどう扱うかです。2025年のレビューでも、CAR-T の cost-effectiveness は適応、比較対照、追跡期間、再発後治療、医療制度差によって大きく変わり、Managed Entry Agreements のようなリスク分担型の仕組みがEUで有力視されていると整理されています。
したがって商業化で本当に問われるのは、単に list price を下げることではなく、
- どの患者群で最も価値が高いか
- その価値をどう測るか
- 初期費用と長期便益の時間差をどう制度的に橋渡しするか
です。
この観点では、毒性管理や再入院率、bridging必要性、V2V、施設滞在期間なども経済評価に組み込まれるべきで、CAR-Tの「勝ち筋」は臨床奏効だけでなく、医療システム負荷を含む総価値提案にあります。
なぜいま in vivo CAR-T に大手が殺到しているのか
このB6の文脈で recent deal を見ると、なぜ大手が in vivo CAR-T に急速に張っているのかが理解しやすくなります。
Orna、Capstan、Interius への関心は、単に「新しい方がすごそう」だからではありません。彼らが狙うのは、apheresis、患者ごと製造、複雑物流、長いV2V、限られた施設キャパといった旧来型の構造欠陥に対して、別の産業設計を持ち込むことです。AbbVie は Capstan の targeted LNP/mRNA に、Kite は Interius の integrating in vivo platform に、Lilly は Orna の circular RNA と in vivo CAR-T/immune reset の将来性に賭けています。これは技術選好というより、商業化アーキテクチャの賭けです。
さらに2026年3月の Nature Medicine 論文で、anti-BCMA in vivo CAR-T のphase 1初期データが示されたことは、この領域が概念段階から臨床現実へ一歩進んだことを意味します。ただし、症例数は5例と小さく、追跡も限定的です。したがって現時点では「すぐ既存CAR-Tを置き換える」と考えるのは早計であり、むしろ 旧来型の完成度向上と、次世代型の実装検証が並走する時期と捉えるのが妥当です。
同種CAR-Tと分散型製造も「勝ち筋」の候補
in vivo CAR-T だけが答えではありません。
同種CAR-Tは、患者ごと製造からの脱却という意味で依然として魅力的です。拒絶、GVHD、持続性など固有課題はありますが、availability と標準化の潜在力は大きいと2025年レビュー群でも整理されています。自己免疫領域での商業可能性を論じたレビューも、同種プラットフォームを重要な選択肢として扱っています。
また、院内または地域分散型の manufacturing も、すべての市場で同じように機能するわけではないにせよ、少なくともアクセス改善の選択肢として無視できなくなっています。B6での本質は、中央集約、分散型、同種、in vivo のどれが唯一の正解かを決めることではありません。重要なのは、どの適応・地域・償還環境・施設密度で、どのモデルが最も摩擦が少ないかを見極めることです。
商業化の勝ち筋:結局、何を持つ企業が強いのか
ここまでを整理すると、CAR-T商業化で強い企業・プラットフォームには共通点があります。
第一に、COGSを下げるだけでなく、COGSと品質の両立設計があること。
第二に、V2V/TATを短く、かつ読める形で運用できること。
第三に、release/QC/CMC/comparability を後追いではなく前提条件として組み込んでいること。
第四に、投与施設の負荷を理解し、導入障壁を下げる運用設計を持つこと。
第五に、承認後のLTFUやデータ取得まで回し切る体制があることです。
言い換えれば、CAR-T商業化の勝ち筋は「最強の細胞を1回作ること」ではありません。
規制に耐え、病院が回せ、payerが受け入れ、患者が間に合う形で、何度でも同じ品質を供給できることです。これができるなら旧来型でも十分強い。逆に、それができないなら、どれほど先端的な設計でも市場では伸びにくい。B6の視点では、CAR-Tはバイオロジーの勝負であると同時に、オペレーションの勝負なのです。
まとめ:CAR-Tの未来は「強い細胞」より「回るシステム」にある
CAR-Tの次の10年を決めるのは、もはや単純なresponse rate競争ではありません。
もちろん有効性は前提ですが、商業化を分けるのは、
COGSをどう圧縮するか
TATをどう短くするか
施設負荷をどう軽くするか
QC/CMC/comparability をどう早期から設計するか
長期追跡と支払いモデルをどう整えるか
という、システムとしての完成度です。
コメント