まず全体像(A3)から読みたい方はこちら:
→ A3:固形がんでCAR-Tが難しい理由(3つの壁)
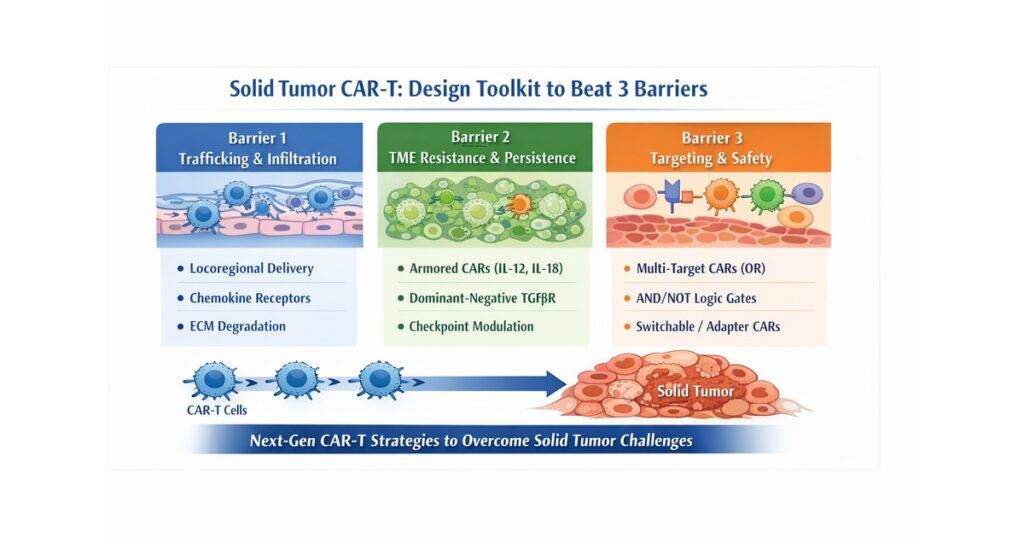
“Solid Tumor CAR-T: Design Toolkit to Beat 3 Barriers”
- Barrier 1: Trafficking/Infiltration
- Barrier 2: TME Resistance/Persistence
- Barrier 3: Targeting/Safety
まず結論(エグゼクティブ・サマリー)
固形がんCAR-Tの本質は、「標的を当てる」だけではなく、A3で述べた **3つの壁(入りにくい/働きにくい/狙いにくい)**に対して、設計で“同時に”勝ちに行くことです。近年の開発トレンドは次の3方向に収束しています。
- 標的×安全性の再設計(多標的・論理ゲート・可変CAR)
- 腫瘍微小環境(TME)に負けない“装甲化”と疲弊対策(cytokine/チェックポイント/抑制シグナル耐性)
- 到達性の再設計(局所投与、遊走・浸潤エンジニアリング、ECM突破)
臨床では、中枢神経系腫瘍(特に再発高悪性度グリオーマ/GBM)で局所投与CAR-Tの安全性と一部の有望シグナルが蓄積しており、「固形がん=全く無理」という段階ではなくなっています。
1) 固形がんCAR-Tの“設計原理”:3つの壁×3つのレバー
固形がんで勝ち筋があるプログラムは、だいたい以下の「掛け算」をしています。
壁① 入りにくい(Trafficking/Infiltration)
- レバーA:局所投与(腫瘍/髄腔内、肝動注、胸腔内など)
- レバーB:遊走の強化(chemokine receptorなど)
- レバーC:浸潤の強化(ECM/間質の突破)
壁② 働きにくい(TME/Exhaustion)
- レバーA:装甲化(Armored/TRUCK)(IL-12/IL-18等、局所で免疫を立ち上げる)
- レバーB:抑制シグナル耐性(dominant-negative receptors、checkpoint rewiring)
- レバーC:持続性/代謝の最適化(疲弊しにくいT細胞設計)
壁③ 狙いにくい(Target/Safety/Heterogeneity)
- レバーA:多標的(OR)(抗原逃避の抑制)
- レバーB:論理ゲート(AND/NOT)(正常組織リスクを下げる)
- レバーC:アダプター/スイッチ式CAR(投与量で活性を制御)
この「3×3」を頭に入れておくと、固形がんCAR-Tの論文・企業資料の読み解き速度が上がります。
2) 壁③(標的と安全性)を解く:固形がんでは“シングル標的”が敗因になりやすい
固形がんで最初に詰まるのは、理想的標的(腫瘍のみ・均一発現)が少ないことです。ここでの最重要トレンドが 多標的化 と 論理ゲート化 です。
2-1. ORゲート(多標的):抗原逃避を減らす
- 同一CARに複数標的(tandem/bicistronic)を持たせ、どちらかがあれば攻撃
- 意味:腫瘍内の標的不均一性に耐える
- トレードオフ:正常組織発現を拾うリスクが上がることがある
ORゲートは、固形がんの“抗原逃避”を減らす有望アプローチとして広く論じられています。
2-2. ANDゲート(論理ゲート):安全性と特異性を上げる
- 2つの条件がそろった時だけ強く活性化
- 代表例:synNotch(一次抗原で“起動”→二次抗原で“攻撃”)や、分割受容体など
論理ゲートは「固形がんの標的が完璧ではない」現実への工学的回答です。
2-3. NOTゲート(iCAR等):正常組織を避ける
- 正常組織に多い抗原を“抑制シグナル”として利用し、正常側でブレーキ
- 目的:オンターゲット・オフ腫瘍毒性の低減
2-4. アダプターCAR(ユニバーサル/スイッチ式):投与で制御する
- CAR-T側は共通受容体、外から入れる“アダプター分子”で標的を指定
- 目的:止められる、標的を変えられる、強度を調整できる
- 実務的に強い:安全性と運用性の武器になる
3) 壁②(TME/疲弊)を解く:装甲化・抑制耐性・チェックポイント再配線
固形がんで“効かない”最大原因の一つは、TMEでCAR-Tが疲弊し、増えず、続かないことです。ここは設計で勝負ができます。
3-1. 装甲化(Armored CAR / TRUCK)
- CAR-T自身がサイトカインや免疫調整因子を出し、局所で免疫を立ち上げる
- 例:IL-12/IL-18等のサイトカインエンジニアリングが議論される
- 目的:TMEの“免疫停止”を壊し、腫瘍内で戦える場を作る
3-2. 抑制シグナル耐性(dominant-negative / switch receptors)
- TGF-βなど、TMEで強い抑制因子への耐性を持たせる(dominant-negative TGFβR等)
- 抑制を逆に活性化へ変換する“スイッチ受容体”設計も議論される
この領域は「TMEが勝つ構造」を設計で崩す典型例です。
3-3. チェックポイント再配線(PD-1軸など)
- PD-1経路など、疲弊に関わる回路を編集/調整し、機能低下を抑える
- ただし副作用・持続性・腫瘍外影響の評価が必要(過度な一般化は禁物)
4) 壁①(到達性)を解く:局所投与と“走れるCAR-T”の設計
固形がんCAR-Tで臨床的に最も説得力が出やすいのが 局所投与です。到達性を根本から変えるからです。
4-1. 局所投与(locoregional delivery):GBMは“現場の実験場”になっている
IL-13Rα2標的CAR-Tの局所投与(再発高悪性度グリオーマ)で、安全性と一部の有望シグナルが報告されています。
ここから得られる一般化可能な学びは:
- “到達できる場所”ではCAR-Tは戦える
- 腫瘍内T細胞状態(前から存在するT細胞など)が効き方に関係する可能性
- 投与経路は、設計と同じくらい重要
4-2. 遊走エンジニアリング(chemokine receptor等)
- 腫瘍が出すケモカインに合わせて受容体を付け、腫瘍へ“寄せる”
- 実務上の評価点:腫瘍に到達した証拠(トラッキング、腫瘍内検体)
4-3. 浸潤エンジニアリング(ECM/間質の突破)
- 腫瘍間質は“物理的壁”なので、酵素・走化性・細胞状態の工夫で突破を狙う
- ここは毒性・局所炎症とのバランスが難所
5) 標的トレンド:固形がんで何が狙われているか(“代表”を押さえる)
固形がんCAR-Tは腫瘍種別に標的が分かれますが、特にCNS腫瘍では以下が頻出です:IL13Rα2、HER2、EGFR/EGFRvIII、EphA2、GD2、B7-H3 など。
※このシリーズの“適応別ディープダイブ”は、必要なら派生記事として作れます(腫瘍種ごとに1本)。
6) “T細胞以外”の選択肢:CAR-NK / 同種(allogeneic)/ iPSC由来
固形がんでは、T細胞にこだわらず CAR-NKや同種細胞(off-the-shelf)も重要な潮流です。
- allogeneic CARの臨床トレンドや設計戦略が整理されています
- CAR-NKは固形がんの“安全性と供給”の観点で注目される
ただし、固形がんでの持続性・浸潤・TME耐性は、どの細胞種でも課題になり得ます。
7) では“何が次の勝ち筋”か:12–24か月で見るべき触媒(Catalysts)
読者(研究者・投資家・臨床側)が次に追うべき“勝負所”は以下です。
- 局所投与×CNS腫瘍のデータ蓄積(安全性・持続・反応の再現性)
- 論理ゲート/多標的の臨床データ(安全性を保ったまま効果が出るか)
- 装甲化/抑制耐性が“有効性を伸ばし、毒性を増やしすぎないか”
- 供給モデル(同種・CAR-NK)の成熟:TAT/COGS/一貫性の改善
まとめ(B3の要点を1ページで)
- 固形がんCAR-Tは「標的」単独では勝てない
- 勝ち筋は 多標的/論理ゲート(安全性)×装甲化/抑制耐性(TME)×到達性(局所投与/遊走) の掛け算
- “臨床の説得力”が最も出ているのは、現時点では局所投与を含むCNS領域が中心
主要参考(読み物として強い一次/総説)
- 固形がんCAR-Tの現状と設計トレンド総説
- GBM/高悪性度グリオーマの局所投与CAR-T(臨床)
- allogeneic CAR / CAR-NKの臨床動向
コメント