序章:難治がん・膵臓がんの壁
膵臓がん(膵管腺がん, PDAC)は、がん研究の中でも最も手ごわい対象とされています。5年生存率はわずか約10%。多くの患者において診断時には進行しており、外科手術や化学療法を行っても根治は難しいのが現実です。
その背景には、以下の3つの大きな課題が横たわっています。
- KRAS変異の支配
PDACのほぼ全例でKRAS遺伝子に変異が存在し、腫瘍の「エンジン」として働き続けています。 - 薬剤耐性の出現
KRAS阻害剤が近年ようやく開発されましたが、単独投与では一時的な効果にとどまり、やがて耐性や再発が起こります。 - 免疫療法の不発
PDACは免疫抑制的な腫瘍微小環境を持ち、「免疫的に冷たい腫瘍」と呼ばれます。そのため、がん免疫チェックポイント阻害薬(ICI)が劇的な効果を示すメラノーマや肺がんとは異なり、膵臓がんでは効果がほとんど得られていません。
この三重苦を前に、研究者たちはKRAS阻害と免疫療法の融合に活路を見いだそうとしています。それが「Two Shots on Goal(二本立ての攻め)」という新戦略です。
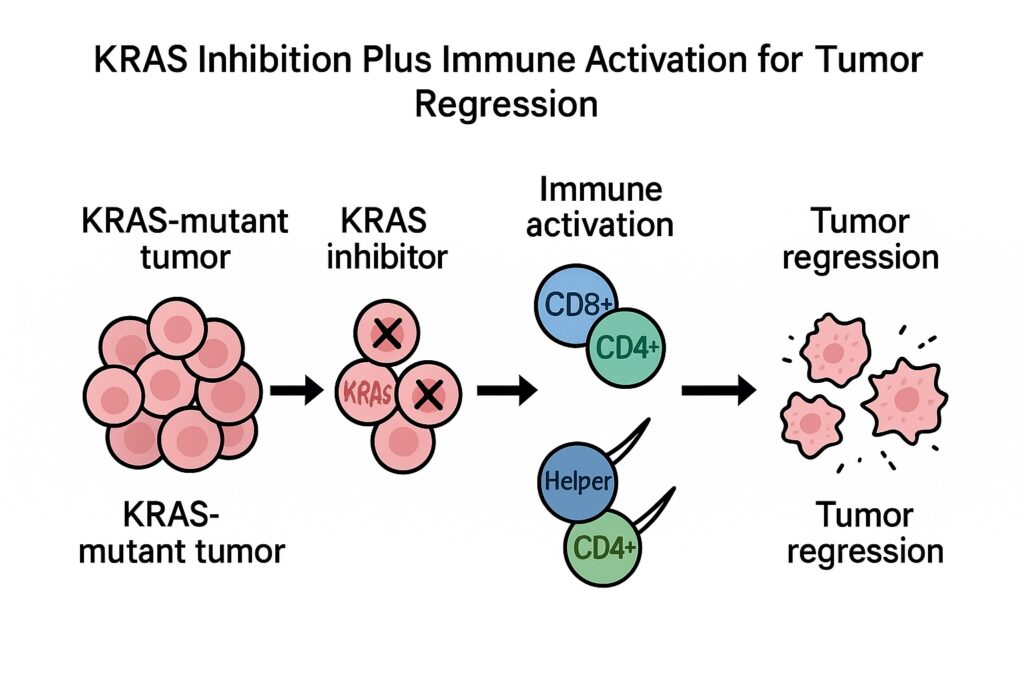
第一の矢:しぶとい残存細胞(persister cells)を“老化”に追い込む
(Broderickら, Memorial Sloan Kettering/RevMed)
KRAS阻害剤によって多くの腫瘍細胞は死滅しますが、一部の細胞はしぶとく生き残り、「persister細胞」として再発の種になります。
この研究では、**RAS(ON) multi-selective阻害剤(RMC-7977)とCDK4/6阻害剤(palbociclib)**を組み合わせました。その結果:
- persister細胞が**老化様状態(senescence-like state)**に固定される。
- これらの細胞は**SASP(炎症性サイトカイン群)**を分泌し、腫瘍微小環境に免疫細胞を呼び寄せる。
- さらにCD40アゴニストを加えると、**CD4 T細胞依存的な腫瘍−免疫均衡(tumor-immune equilibrium)**が成立し、長期にわたる腫瘍抑制を達成。
特に注目すべきは、単剤治療では再発が避けられないマウスPDACモデルで、この3剤併用により持続的な腫瘍退縮と生存延長が確認されたことです。
つまり「腫瘍細胞を殺す」だけでなく「残存細胞を老化させ、免疫に処理させる」という新しい治療コンセプトを提示しました。
第二の矢:KRAS阻害が免疫システムを目覚めさせる
(Orlenら, ペンシルベニア大学/RevMed)
こちらの研究は、「KRAS阻害が免疫環境にどのような影響を与えるか」を中心に検証しました。
主要な成果
- T細胞浸潤が少ない腫瘍では
腫瘍は縮小するが、完全奏効(CR)は得られない。 - T細胞浸潤が豊富な腫瘍では
なんと**90%で完全奏効(CR)**が得られるという劇的な結果。 - 免疫環境の変化
- 抑制的なMDSCの減少
- M1型マクロファージの増加
- CD8+T細胞の浸潤、増殖、メモリー化
- 腫瘍細胞自身がMHC-I発現を増加し「免疫に見つかりやすい」状態に変化
- 免疫療法との併用
KRAS阻害単独を超えて、より深く、より持続的な腫瘍退縮を実現。完全奏効率も飛躍的に高まった。
意義
KRAS阻害は単なる腫瘍抑制剤ではなく、**免疫を目覚めさせる“免疫感作因子”**として機能する可能性を明確に示しました。
コメント論文の視点(Opsahl & Pasca di Magliano)
これら2つの研究を総評する形で発表されたコメント論文は、次のように強調しています:
- KRAS阻害単独は不十分だが、免疫システムとの二重攻撃によって長期寛解が可能になる。
- persister細胞の老化誘導(Broderick)と、T細胞依存的な完全奏効(Orlen)は、異なるアプローチながら同じ結論に至った。
- この二本立ての戦略こそ「Two Shots on Goal」であり、膵がん治療における新しい希望の象徴である。
総括:Two Shots on Goalが切り開く未来
今回の3本の論文から見えてきたのは、膵がん治療における新しい地平です。
- KRAS阻害は直接的な腫瘍殺傷力だけでなく、免疫環境を変える強力な手段である。
- 免疫療法は単独では不発に終わるが、KRAS阻害と組み合わせることで初めて真価を発揮する。
- persister細胞の老化固定と免疫による排除、T細胞依存の腫瘍退縮、この二本立てが揃うことで長期寛解が現実味を帯びる。
この戦略が臨床試験で再現されれば、膵がんの治療史を大きく塗り替える可能性があります。今後は、KRAS阻害剤の改良、免疫活性化薬の最適な組み合わせ、そして適切な患者層の特定が焦点となるでしょう。
参考文献
- Cancer Discovery, Vol.15, No.8 (2025).
“Two Shots on Goal: Combination of RAS Inhibition and Immunotherapy Drives Long-term Remission in Pancreatic Cancer”
Emily L. Lasse Opsahl - Cancer Discovery, Vol.15, No.8 (2025).
“A RAS(ON) Multi-Selective Inhibitor Combination Therapy Triggers Long-term Tumor Control through Senescence-Associated Tumor-Immune Equilibrium in Pancreatic Ductal Adenocarcinoma”
Caroline Broderick - Cancer Discovery, Vol.15, No.8 (2025).
“T-cell Dependency of Tumor Regressions and Complete Responses with RAS(ON) Multi-selective Inhibition in Preclinical Models of Pancreatic Ductal Adenocarcinoma”
Margo Orlen




この記事はMorningglorysciencesチームによって編集されました。









コメント