要点まとめ
- 2026年4月16日 Nature 誌に、慢性炎症(大腸炎)が腸幹細胞のクロマチンに 「エピジェネティック記憶」 として残り、100日以上経過しても消えないことを示す重要論文(Nagaraja et al., Harvard / Broad / MIT, Nature 2026;652:774)が掲載されました。第1回の progenitor niche、第2回の髄芽腫オルガノイドに続く、がん起源研究の第三の視点——「炎症の記憶」を解明した研究です。
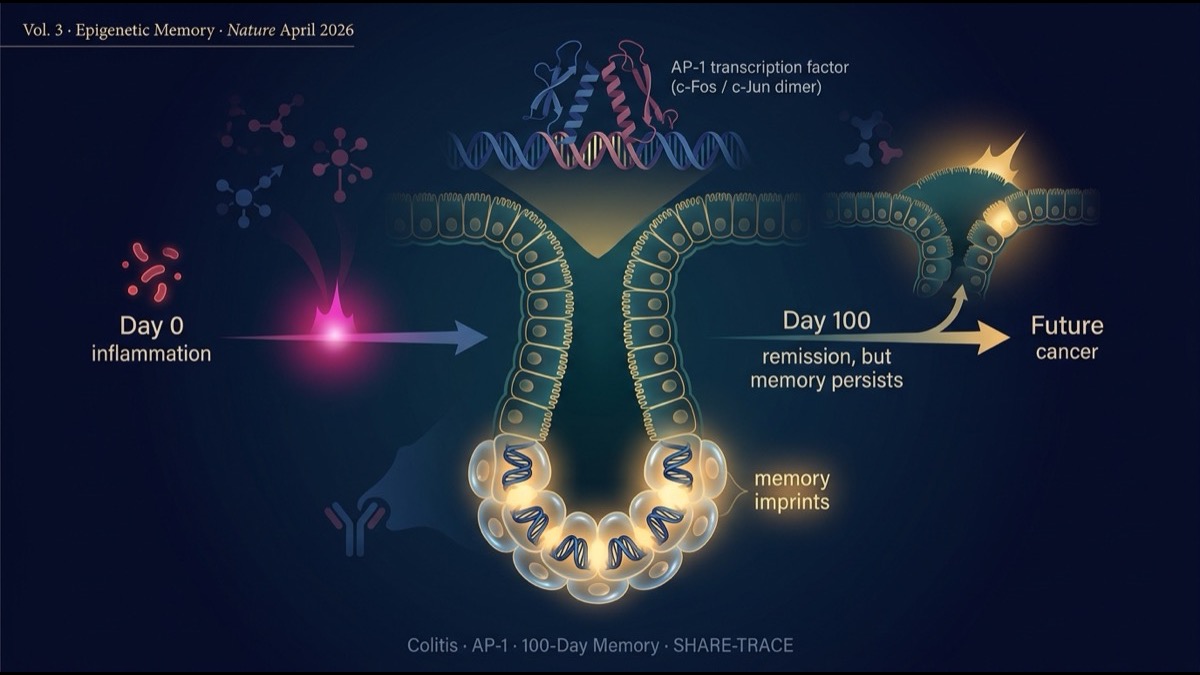
- 機序の核心は、AP-1 転写因子複合体の累積活性。大腸炎発症中に AP-1(c-Fos/c-Jun ダイマー)依存のクロマチン変化が腸幹細胞に蓄積し、寛解後も 100日以上にわたって持続。後続の発がん変異(KRAS、APC等)が起こると、この「記憶」と協調して腫瘍形成を加速します。
- 研究グループは SHARE-TRACE という新しい単細胞技術を開発しました。遺伝子発現、クロマチンアクセス、クローン系統を 同時に1細胞で測定 可能。これにより「記憶を持つクローン vs 持たないクローン」を直接比較し、エピジェネティック記憶が 幹細胞分裂を介してクローン的に継承される ことを証明しました。
- 臨床的含意:炎症性腸疾患(IBD、潰瘍性大腸炎、クローン病)患者の大腸がんリスク上昇は、長らく「炎症 → 発がん」の直線的因果関係で語られてきました。本論文は 「炎症の記憶 + 後続変異」という協調モデル を提示し、IBD 関連がん予防戦略の設計を変える可能性を持ちます。AP-1 阻害は新しい治療軸として浮上します。
序論——「炎症ががんを促す」をどう測るか
慢性炎症が発がんリスクを上げる、という臨床観察は古くから知られています。例えば:
- 慢性ヘリコバクター・ピロリ感染 → 胃がん(5-10倍リスク)
- 慢性 B/C 型肝炎 → 肝細胞がん(10-100倍リスク)
- 炎症性腸疾患(IBD:潰瘍性大腸炎、クローン病) → 大腸がん(2-5倍リスク、罹患期間に比例)
- 慢性膵炎 → 膵がん(リスク上昇)
これら観察は、「炎症が直接的に DNA 損傷を起こし、変異が累積して発がんする」という単純モデルで説明されてきました。確かに、活性酸素(ROS)による DNA 損傷、炎症性サイトカインの直接変異原性、組織再生のための過剰な細胞分裂による複製エラー——これらは部分的に正しい説明です。
しかし、過去5年間のエピジェネティクス研究は、別の機序を浮上させてきました。「炎症は遺伝子配列を変えるだけでなく、ゲノムの『使い方』を変える」という可能性。具体的には、ヒストン修飾、DNA メチル化、クロマチンアクセス性が変化し、変異がなくても遺伝子発現プロファイルが変わり、がんに繋がる、という機序です。
2026年4月号 Nature 誌の Nagaraja et al. の論文は、この「炎症のエピジェネティック効果」が 幹細胞のクロマチンに長期記憶として残る という驚くべき発見を報告しました。さらに、その記憶が後続の発がん変異と協調することを、新しい単細胞技術 SHARE-TRACE で因果的に証明しました。
本記事は、本論文の研究戦略・主要結果・機序・臨床応用可能性を順に解説し、後半でグローバル研究・産業への含意をまとめます。
本論
1. 炎症性腸疾患と大腸がんの疫学
本論文を読み解く前に、IBD関連大腸がんの臨床的重要性を確認します。
潰瘍性大腸炎・クローン病患者は、罹患期間が長くなるほど大腸がんリスクが上がります。代表的な数字(Eaden et al. Gut 2001、Dyson et al. Aliment Pharmacol Ther 2012 等):
- 10年罹患:約2倍
- 20年罹患:約8倍
- 30年罹患:約18倍
このため IBD 患者には定期的な大腸内視鏡サーベイランスが推奨されています。しかし、「なぜ罹患期間に比例してリスクが上がるのか」 の分子機序は不明確でした。
古典的説明は「累積的炎症 → 累積的 DNA 損傷 → 累積的変異」。しかし、これだけでは 「炎症が寛解した後もリスクが残る」という臨床所見を完全に説明できません。寛解した時点で炎症は止まっているはず——ところが、リスクは残る。何かが「記憶」されているはずです。
2. マウス大腸炎モデルで「記憶」を捕捉する
研究グループは、デキストラン硫酸ナトリウム(DSS)誘発大腸炎モデルを使いました。マウスに DSS を含む水を5日間飲ませ、急性大腸炎を誘発。その後 100日以上、通常飼料で飼育して炎症を完全寛解させます。
このモデルで以下を測定:
- 炎症期:急性大腸炎発症中の腸幹細胞
- 初期寛解期:炎症消失直後(10日後)
- 長期寛解期:100日以上経過した「炎症痕跡なし」状態
各タイミングで腸幹細胞(Lgr5+)を単離し、クロマチンアクセス性(ATAC-seq)、ヒストン修飾(CUT&RUN)、転写プロファイル(RNA-seq)を測定。
3. 主要発見1:100日後にも残るクロマチン変化
結果は驚くべきものでした。炎症発症100日後の腸幹細胞は、外見上は完全に健常マウスと区別できない。組織学的にも臨床的にも炎症は完全に治っている。しかし、ゲノムワイドのクロマチン解析では、炎症経験を持たないコントロール幹細胞とは明らかに異なるアクセス性プロファイル を示しました。
具体的には:
- 炎症関連遺伝子座のクロマチンが「開いた」状態を維持
- NF-κB、AP-1、STAT 経路の標的遺伝子座のアクセス性が亢進
- ヒストン修飾では H3K27ac(活性エンハンサーマーク)が炎症関連エンハンサーで持続的に高発現
- 遺伝子発現レベルでは、これら遺伝子は「必要時に強く発現する準備状態」にある
つまり、腸幹細胞は炎症経験を 「クロマチン構造の中に記憶」 していたのです。普段は静かだが、刺激があれば即座に強く反応する状態。
4. AP-1 が「記憶を書く酵素」だった
このエピジェネティック記憶の中心役を担うのは何か? 研究グループは、複数のクロマチン解析と機能阻害実験から AP-1 転写因子複合体(c-Fos / c-Jun のダイマー)を特定しました。
AP-1 は古典的な「即時応答遺伝子」を担当する転写因子で、ストレス・炎症・成長因子刺激に応答して急速に活性化します。研究の発見:
- 炎症期に AP-1 結合部位のクロマチンが大規模に「開く」
- 炎症消失後も、AP-1 結合部位の 「開いた状態」が維持 される
- これら部位の周囲では H3K27ac が長期維持され、エンハンサーとして潜在的に機能
- AP-1 活性を遺伝学的に阻害(c-Fos/c-Jun の機能阻害)すると、記憶形成が阻害される
つまり AP-1 は「炎症経験をクロマチンに書き込む酵素」として機能していました。
5. SHARE-TRACE:3つを同時測定する新技術
研究の白眉は、この記憶が 「幹細胞分裂を介してクローン的に継承される」ことを証明した点。これには新しい技術 SHARE-TRACE が必要でした。
SHARE-TRACE は1個の細胞から:
- 転写プロファイル(scRNA-seq 相当)
- クロマチンアクセス性(scATAC-seq 相当)
- クローン系統情報(CRISPR バーコード追跡)
を 同時測定 する技術。この三冠データから、「同じ起源クローンの娘細胞同士で、炎症記憶(クロマチン特徴)が共有されているか」を直接判定できます。
結果、同一起源クローンに属する娘細胞群は、炎症記憶のクロマチン特徴を統計的に高頻度で共有 していました。さらに、クローンによって記憶の強度が異なる——つまり「強い記憶を持つクローン」と「弱い記憶を持つクローン」が共存し、強い記憶を持つクローンは経世代的に記憶を継承することが示されました。
6. 主要発見2:記憶が発がん変異と協調する
記憶があるだけでは「がん」にはなりません。研究グループは、記憶を持つマウスに発がん変異(APC機能喪失)を導入する 実験で、記憶と変異の協調を測定しました。
結果:
- 記憶あり(DSS 経験あり) + APC 変異 → 大腸腫瘍が 顕著に多く・大きく 形成
- 記憶なし(DSS 経験なし) + APC 変異 → 通常レベルの腫瘍形成
- 記憶あり + AP-1 阻害 + APC 変異 → 腫瘍形成が 記憶なしレベルに減弱
つまり、「炎症記憶」は単独では発がんを起こさないが、後続の発がん変異と組み合わさると 腫瘍形成を顕著に加速 します。AP-1 を阻害すれば、この加速効果は消失します。
7. 機序:AP-1 標的遺伝子プログラムが発がんを加速する
記憶 + 変異が腫瘍を加速する分子レベルの理由は何か? 研究グループは:
- 記憶あり + APC 変異マウスの腫瘍細胞で、AP-1 標的遺伝子プログラムの発現が顕著に上昇
- これら標的には増殖(cyclin D1、Myc)、上皮間葉転換(Snail、Slug)、細胞外マトリクスリモデリング(MMP9)が含まれる
- つまり、APC 変異が WNT/β-catenin を活性化し、増殖シグナルを供給。同時に、記憶クロマチンが AP-1 標的遺伝子を「開いた」状態に保ち、強い発現で増殖を加速。
このダブルアクセル機構が、「IBD 関連がんが通常の散発性大腸がんより速く・侵襲的に進展する」という臨床所見の分子的説明を提供しました。
8. 臨床的含意:AP-1 阻害という新治療軸
本論文の臨床的含意は3つ:
第一に、IBD 関連がんの予防戦略。長期罹患 IBD 患者で、定期サーベイランスに加えて 「AP-1 経路を抑える化学予防」という新概念。AP-1 直接阻害薬は限定的だが、間接的に AP-1 を抑制する既存薬(JAK 阻害薬、メラノコルチン経路活性化薬)の応用研究が動き始めています。
第二に、長期寛解 IBD 患者のリスク層別化。「クロマチン記憶の強さ」を検出するバイオマーカーが開発されれば、「強い記憶を持つ患者」をリスク高群として特定し、より頻繁なサーベイランスや化学予防の対象に。便由来 DNA メチル化アッセイ、血液中の AP-1 標的遺伝子発現プロファイル等が候補。
第三に、確立した IBD 関連がんへの新治療軸。すでに発がんしている患者でも、AP-1 経路を阻害すれば、増殖駆動メカニズムの一部を解除できる可能性。WNT 経路阻害薬(PORCN 阻害)と組み合わせる治療設計が考えられます。
9. 限界と注意点
本論文には以下の限界があります。
第一に、マウスからヒトへの一般化。マウスの記憶機序が同じ強度・持続でヒトでも機能するかは、ヒト IBD 患者のシリアル生検でのクロマチン解析が必要。
第二に、AP-1 単独か複数経路の協調か。NF-κB、STAT3、HIF-1α 等他の炎症経路もエピジェネティック記憶に寄与する可能性。
第三に、ヘリコバクター・ピロリと胃がん、HBV/HCVと肝がん等、他の慢性炎症-がん関係でも同じ機序が働くか。AP-1 の関与は文脈依存。
第四に、AP-1 阻害の毒性懸念。AP-1 は正常細胞の創傷治癒、免疫応答、組織再生にも必須。慢性投与による副作用評価が必要。
まとめ
- Nagaraja et al. Nature 2026 は、慢性大腸炎が腸幹細胞のクロマチンに AP-1 依存のエピジェネティック記憶 を残し、100日以上持続することを示した。
- 新技術 SHARE-TRACE(転写・クロマチン・系統の3冠単細胞測定)で、この記憶が 幹細胞分裂を介してクローン的に継承 されることを証明。
- 記憶単独では発がんしないが、後続の発がん変異(APC機能喪失)と協調 すると腫瘍形成を顕著に加速。AP-1 阻害でこの加速は消失。
- 分子機序は、APC 変異による WNT 活性化+記憶クロマチン由来の AP-1 標的遺伝子プログラム強発現の ダブルアクセル。
- 臨床応用:AP-1 阻害化学予防、クロマチン記憶バイオマーカー、確立 IBD 関連がんへの新治療軸。
- 限界:マウス → ヒト一般化、AP-1 単独 vs 多経路協調、他のがん種への拡張可能性、AP-1 阻害の毒性。
シリーズ総括
連載「がん細胞起源研究の最前線」3部構成を通して、私たちは2026年4月の3本の重要論文を解剖してきました。
第1回では Reyes et al.(Cell)の progenitor niche モデル——変異だけではがんにならず、特定の前駆細胞集団が「自己強化型ニッチ」を形成する転換点が必要、という構造的洞察。
第2回では Cell の髄芽腫オルガノイド論文——マウスでは再現できないヒトがんを、iPSC + CRISPR でリアルタイム再現する新世代モデル。
第3回(本記事)では Nagaraja et al.(Nature)のエピジェネティック記憶論文——慢性炎症が幹細胞クロマチンに長期記憶として残り、後続変異と協調する第三の視点。
これら3つの研究は、それぞれ 空間(ニッチ)、時間(発生過程)、記憶(炎症痕跡)という3つの軸で、がん起源研究をパラダイム転換させています。共通するのは、「変異の蓄積だけでがんになるわけではない」という結論。組織レベルの動的状態、発生過程の特定タイミング、過去の経験の痕跡——これら非変異的要素ががん発生を駆動する。これは、がん予防医療、早期介入、リスク層別化、新規治療標的の議論を構造的に書き換える発見の集合です。
私の考察・展望
連載総括として、最も大きな示唆は 「がん発生研究は、変異中心のジェネティクスから、組織と時間と経験を統合する『コンテクスチャル・オンコロジー』へとパラダイムシフトしている」という事実です。研究者と業界観察者の立場でこの分野を見てきた率直な感覚として、過去20年がDNA配列解析と変異カタログ化の時代だったとすれば、これからの10年は シングルセル空間オミクス、オルガノイドモデル、エピジェネティック動的解析 の統合時代です。
日本の研究・産業にとっての示唆は3点。第一に、炎症性腸疾患臨床の蓄積。日本は世界トップクラスの IBD 臨床研究センター(東京医科歯科大、慶應、北海道大、九大、大阪医科薬科大等)を持ち、患者コホート、内視鏡サーベイランス、生検サンプルバンクが整備されています。Nagaraja ら の所見を日本人 IBD コホートで再現する研究は、世界貢献できる立ち位置にあります。第二に、エピジェネティック診断・治療技術。日本のオルガノイド・エピジェネティクス研究(理研IMS、京大iPS研究所、阪大微研)の蓄積は、IBD 関連がんバイオマーカー診断キット開発に直結します。第三に、AP-1 経路阻害薬の探索。武田、第一三共、エーザイのアセット・ライブラリにおける AP-1 経路標的化合物の再評価が、新しいがん予防薬の発掘につながる可能性。
シリーズ全体を読了していただいた皆様と、この「コンテクスチャル・オンコロジー」革命を今後も共有していければと願っています。
Morningglorysciencesチームによって編集されました。




コメント